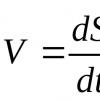Скорость химических реакций. Характеристика окислительно-восстановительных свойств серной кислоты. Получение тиосульфата натрия A) Влияние силы кислоты и основания, образующих соль, на степень её гидролиза
Описание продукта
Гипосульфит натрия внешне выгледит в виде бесцветных кристаллов, которые хорошо растворяются в воде. Он широко применяется в промышленности и медицине. Считается сильным восстановителем.
Гипосульфиты (тиосульфаты) неустойчивы, поэтому в природе не встречаются.
Химическая формула
: Na2S2O3 или Na2SO3S
Синонимы
: тиосульфа́т на́трия, антихлор, сульфидотриоксосульфат натрия, натрий серноватистокислый.
Применение гипосульфата (тиосульфата) натрия.
Его применяют, чтобы удалить следы хлора после отбеливания тканей, для быстрого извлечения серебра из руд, фиксажа в фотографии, в качестве реактива в иодометрии, противоядия при отравлениях токсичной ртутью, а также другими тяжёлыми металлами, цианидами.
В годы первой мировой войны гипосульфитом пропитывали марлевые повязки и фильтры противогазов для защиты органов дыхания от ядовитого хлора. Его же используют в качестве реактива в аналитической и органической химии, им нейтрализуют сильные кислоты, обезвреживают тяжелые металлы и их токсические соединения. Реакции взаимодействия тиосульфата с различными веществами являются основой йодометрии и бромометрии.
В медицине гипосульфит натрия используется для дезинфекции кишечника, лечения чесотки, в качестве противовоспалительного и противоожогового средства. Также используется как оптимальная среда для определения молекулярных весов по понижению точки замерзания.
В пищевой промышленности гипосульфит натрия зарегистрирован в качестве пищевой добавки E539. Особенно часто его применяют в пекарском производстве. Гипосульфит натрия делает тесто более пластичным, а хлеб становится более рыхлым и объемным. На поверхности изделия не формируются трещины, а выпечка приобретает более привлекательный внешний вид. Количество ввода в состав зависит от вида хлеба и составляет от 0,001 до 0,002 процента от общего веса муки.
В фотографии
использование гипосульфита (тиосульфата) натрия в качестве фиксажа основана на способности тиосульфат-иона переводить нерастворимые в воде светочувствительные ионы серебра в растворимые несветочувствительные комплексы.
Фиксажи условно делятся на нейтральные, кислые, дубящие и быстрые.
Нейтральный фиксаж представляет собой раствор тиосульфата натрия в воде. Для упрочнения эмульсионного слоя фотографии используют дубящие фиксажи.
В качестве дубящих веществ в разных рецептурах могут использоваться тетраборат натрия, борная кислота, хромокалиевые или алюмокалиевые квасцы и формалин.
веществ в разных рецептурах могут использоваться тетраборат натрия, борная кислота, хромокалиевые или алюмокалиевые квасцы и формалин.
В кожевенном производстве свойство дубящих фиксажей с успехом применяют при выделке кожевенно-мехового полуфабриката на этапе дубления. Такое дубление называют серным. Гипосульфит под воздействием добавляемой в состав раствора кислоты выделяет серу, которая обволакивает коллагеновую структуру волокон в толще шкуры. В результате мездра получается мягкой и пластичной. Шкуры выдубленные с помощью гиросульфта (тиосульфата) натрия, не уступают по качеству изделиям, выделанным алюминием или хромом.
В текстильной промышленности гипосульфит применяют для удаления следов хлора после отбеливания тканей.
Технические характеристики
| Массовая доля, % |
Гипосульфит натрия (фото) |
Гипосульфит натрия (технический) |
|---|---|---|
| Тиосульфата натрия (Na 2 S 2 O 3 · 5H 2 O), мин. | 99,0 | 98,5 |
| нерастворимых в воде веществ, макс. | 0,01 | 0,03 |
| железа (Fe), макс. | 0,001 | 0,002 |
| сернистого натрия (Na 2 S), макс. | 0,001 | 0,001 |
| кальция, магния и веществ, нерастворимых в аммониевых растворах, макс. | 0,02 | не норм. |
| тяжелых металлов (Pb), макс. | 0,001 | не норм. |
| pH водного раствора при 20 о С, макс. | 6,5-9,5 | не норм. |
| внешний вид водного раствора | бесцветный, прозрачный. | не норм. |
Где купить гипосульфит (тиосульфат) натрия?
Гипосульфит натрия (тиосульфат натрия) в фасовках 100г., 250г., 500г., 1кг. продается в Новосибирске в интернет магазине "Для дела". В рабочие часы забрать его можно самовывозом или воспользоваться услугами курьера. Для покупателей из других регионов эта продукция отправляется Почтой РФ или транспортными компаниями.
Тиосерная кислота - неорганическое соединение, двухосновная сильная кислота с формулой H 2 SO 3 S, бесцветная вязкая жидкость, реагирует с водой. Термически неустойчива.Быстро, но не мгновенно, разлагается в водных растворах. В присутствии серной кислоты разлагается мгновенно.
Образует соли - тиосульфаты.Тиосульфа́ты - соли и сложные эфиры тиосерной кислоты, H 2 S 2 O 3 . Тиосульфаты неустойчивы, поэтому в природе не встречаются. Наиболее широкое применение имеют тиосульфат натрия(Na 2 S 2 O 3) и тиосульфат аммония ((NH 4) 2 SO 3 S).
Получение тиосерной кислоты: 1) Реакция сероводорода и триоксида серы в этиловом эфире при низких температурах: ; 2) Действие газообразного хлористого водорода на тиосульфат натрия:
Химические свойства тиосерной кислоты:
1)Термически очень неустойчива:
2)В присутствии серной кислоты разлагается:
3)Реагирует с щелочами:
4)Реагирует с галогенами:
Тиосульфаты получаются:
1) при взаимодействии растворов сульфитов с сероводородом:
2)При кипячении растворов сульфитов с серой:
3)При окислении полисульфидов кислородом воздуха: ,
Химические свойства тиосульфатов:
1)При нагревании до 220 °C распадается по схеме:
2)Тиосульфаты - сильные восстановители:С сильными окислителями, например, свободным хлором, окисляется до сульфатов или серной кислоты:
3)Более слабыми или медленно действующими окислителями, например, иодом, переводится в соли тетратионовой кислоты:
4)Выделить тиосерную кислоту (тиосульфат водорода) реакцией тиосульфата натрия с сильной кислотой невозможно, так как она неустойчива и тут же разлагается:
5)Расплавленный кристаллогидрат Na 2 S 2 O 3 ·5H 2 O очень склонен к переохлаждению.
Практическое применение тиосульфата натрия: в фотографии,аналитической и органической химии,горнорудной промышленности, текстильной и целлюлозно-бумажной промышленности, пищевой промышленности, медицине.
Биологическая роль серы: Как и элементы органогены, сера в виде отдельного элемента не обладает биологическим значением. Ее биологическая роль состоит в том, что она входит в структуру таких аминокислот, как цистеин и метионин, которые и выполняют в животных организмах (в том числе у человека), ряд незаменимых функций.
Круговорот серы в природе: Растения получают ее из почвы в виде серной кислоты; во всяком другом виде сера для зеленых растений недоступна. В теле растения серная кислота путем сложных, пока еще не разъясненных химических преобразований служит материалом для построения белковых веществ, в которых сера находится уже в совершенно иной форме, чем в серной кислоте. В то время, как сера в виде серной кислоты соединена с кислородом, газом, находящимся в воздухе и поддерживающим всякое горение и дыхание, в белках сера уже оторвана от кислорода и соединена с другим элементом с углеродом, который сам по себе представляет обыкновенный уголь. При разложении белков после смерти животного или растения, гнилостные бактерии отрывают серу из белков и выпускают ее в соединении с новым элементом водородом. В таком соединении сера представляет собой тот отвратительный вонючий газ, обладающий запахом тухлых яиц, который всегда образуется при гниении белков и о котором уже была речь раньше. В виде сероводорода сера и попадает в почву.
15. Химия элементов 5 А группы. Распространенность в природе, минералы. Водородные и кислородные соединения. Оксиды и гидроксиды различных степеней окисления. Изменение кислотно-основных и окислительно-восстановительных свойств соединений мышьяка, сурьмы и висмута в степенях окисления +3 и +5.
Химия элементов 5 А группы: В группу входят азот N, фосфор P, мышьяк As, сурьма Sb и висмут Bi . Элементы главной подгруппы V группы, имеют пять электронов на внешнем электронном уровне. В целом характеризуются как неметаллы. Способность к присоединению электронов выражена значительно слабее, по сравнению с халькогенами и галогенами. Все элементы подгруппы азота имеют электронную конфигурацию внешнего энергетического уровня атома ns²np³ и могут проявлять в соединениях степени окисления от −3 до +5 . Вследствие относительно меньшей электроотрицательности связь с водородом менее полярна,чем связь с водородом халькогенов и галогенов. Водородные соединения этих элементов не отщепляют в водном растворе ионы водорода, иными словами, не обладают кислотными свойствами. Первые представители подгруппы - азот и фосфор - типичные неметаллы, мышьяк и сурьма проявляют металлические свойства, висмут - типичный металл. Таким образом, в данной группе резко изменяются свойства составляющих её элементов: от типичного неметалла до типичного металла. Химия этих элементов очень разнообразна и, учитывая различия в свойствах элементов, при изучении её разбивают на две подгруппы - подгруппу азота и подгруппу мышьяка.
Распространенность в природе, минералы. Азот - важнейшая составная часть атмосферы (78% ее объема). В природе встречается в белках, в залежах нитрата натрия. Природный азот состоит из двух изотопов: 14 N (99,635% массы) и 15 N (0,365% массы).Фосфор входит в состав всех живых организмов. В природе встречается в виде минералов. Фосфор широко применяется в медицине, сельском хозяйстве, авиации, при добыче драгметаллов.Мышьяк, сурьма и висмут распространены достаточно широко, в основном в виде сульфидных руд. Мышьяк - один из элементов жизни, способствующий росту волос. Соединения мышьяка ядовиты, но в малых дозах могут оказывать лечебное свойства. Мышьяк применяется в медицине и ветеринарии.
Водородные и кислородные соединения.1)Для азота известны оксиды , отвечающие всем его положительным степеням окисления (+1,+2,+3,+4,+5): N 2 O, NO, N 2 O 3 , NO 2 , N 2 O 4 , N 2 O 5 . При обычных условиях азот с кислородом не взаимодействует, только при пропускании через их смесь электрического разряда. Молекула азотной кислоты HNO 3 состоит из трех элементов, соединенных между собой ковалентными связями. Это молекулярное вещество, содержащее предельно окисленный атом азота. Однако валентность азота в кислоте равна четырем вместо обычной степени окисления азота. Аммиак - одно из важнейших водородных соединений азота. Он имеет огромное практическое значение. Жизнь на Земле во многом обязана некоторым бактериям, которые могут перерабатывать азот воздуха в аммиак.2)Соединения фосфора с водородом представляет собой газообразный фосфористый водород, или фосфин PH 3 (бесцветный ядовитый газ с чесночным запахом, воспламеняется на воздухе). У фосфора несколько оксидов: оксид фосфора (III) P 2 O 3 (белое кристаллическое вещество, образуется при медленном окислении фосфора в условиях недостатка кислорода, ядовит) и оксид фосфора (V) P 2 O 5 (образуется из P 2 O 3 при его нагревании, растворим в воде с образованием фосфористой кислоты средней силы) наиболее важные. Наиболее характерный свойством второго является гигроскопичность (поглощение паров воды из воздуха), при этом он расплывается аморфную массу HPO 3 . При кипячении P 2 O 5 образуется фосфорная кислота H 3 PO 4 (белое кристаллическое вещество, расплывается на воздухе, t пл =42,35 о С,не ядовита, растворима в воде, электролит, получают, окисляя 32%-ую азотную кислоту). Фосфаты почти всех металлов (кроме щелочных) нерастворимы в воде. Дигидрофосфаты хорошо растворимы в воде.
Оксиды и гидроксиды различных степеней окисления. N 2 O, NO, N 2 O 3 , NO 2 , N 2 O 4 , N 2 O 5 ,P 2 O 3, P 2 O 5, P 2 O 3,As2O3, As2O5, Sb2O3, Sb2O5, Вi2О3, Вi2О5, Вi(ОН)3.
Изменение кислотно-основных и окислительно-восстановительных свойств соединений мышьяка, сурьмы и висмута в степенях окисления +3 и +5.
Азот, нахождение в природе. Соединение с водородом,галогенами, кислородом. Аммиак, получение, свойства и его соли. Азотоводородная кислота, соли азиды. Амиды, имиды и нитриды металлов.Биологическая роль азота.
Азо́т - 1s 2 2s 2 2p 3. Элемент 15-й группы (по устаревшей классификации - главной подгруппы пятой группы) второго периода периодической системы химических элементов Д. И. Менделеева, с атомным номером7. Обозначается символом N . Простое вещество азот - достаточно инертный при нормальных условиях двухатомный газ без цвета, вкуса и запаха (формула N 2), из которого на три четверти состоит земная атмосфера.
Нахождение в природе: В большой части азот находится в природе в свободном состоянии. Свободный азот является главной составной частью воздуха, который содержит 78, 2 % (об.) азота. Над одним квадратным километром земной поверхности в воздухе находиться 8 млн. т азота. Общее содержание его в земной коре оценивается величиной порядка 0.03 мол. доли, % . Азот входит в состав сложных органических соединений- белков, которые входят в состав всех живых организмов. В результате отмирания последних и тления их останков образуются более простые азотные соединения, которые при благоприятных условиях, (главным образом - отсутствие влаги) могут накапливаться. Именно такого происхождения, по – видимому, залежи NaNO3в Чили, имеющие некоторое промышленное значение в производстве связанного азота, то есть в виде соединений. Также в природе встречается такой минерал, как индийская селитра K NO3 . По словам известного советского микробиолога В. Л. Омелянского, «азот более драгоценен с общебиологической точки зрения, чем самые редкие из благородных металлов».
Соединение с водородом,галогенами, кислородом:1) Аммиак - соединение азота с водородом. Имеет важное значение в химической промышленности. Формула аммиака - NH5.2) Азотная кислота HNO3 - сильная одноосновная кислота. В разбавленных растворах она полностью распадается на ионы Н* и NO.3) С галогенами азот непосредственно не реагирует, косвенными путями получены NF 3 , NCl 3 , NBr 3 и NI 3 , а также несколько оксигалогенидов (соединений, в состав которых, кроме азота, входят атомы и галогена, и кислорода, например, NOF 3).Галогениды азота неустойчивы и легко разлагаются при нагревании (некоторые - при хранении) на простые вещества. Так, NI 3 выпадает в осадок при сливании водных растворов аммиака и иодной настойки. Уже при легком сотрясении сухой NI 3 взрывается:2NI 3 = N 2 + 3I 2 . 4) Для азота известны окислы, по составу формально отвечающие всем валентностям от. единицы до пяти: N2 O – закись азота, NO – окись азота, N2 O3 – азотистый ангидрид, NO2 – двуокись азота, N2 O5 – азотный ангидрид.
Аммиак, получение, свойства и его соли.Аммиак - соединение азота с водородом. Имеет важное значение в химической промышленности. Формула аммиака - NH5.
Получение аммиака
1) В промышленности получение аммиака связано с прямым его синтезом из простых веществ. Как уже отмечалось, источником азота служит воздух, а водород получают из воды.3H 2 + N 2 -> 2NH 3 + Q .2) Получение аммиака в лабораторных условиях производят из смеси твёрдого хлорида аммония (NH 4 Cl) и гашенной извести. При нагревании интенсивно выделяется аммиак.2NH 4 Cl + Ca(OH) 2 -> CaCl 2 + 2NH 3 + 2H 2 O.
Свойства аммиака: 1)присоединяет протон, образуя ион аммония:
2) Взаимодействуя с кислотами даёт соответствующие соли аммония:
3) Амиды щелочных металлов получают, действуя на них аммиаком:
4) Амиды являются более сильными основаниями, чем гидроксиды, а следовательно, подвергаются в водных растворах необратимому гидролизу:
5) При нагревании аммиак проявляет восстановительные свойства. Так, он горит в атмосфере кислорода, образуя воду и азот. Окисление аммиака воздухом на платиновом катализаторе даёт оксиды азота, что используется в промышленности для получения азотной кислоты:
6) Окисляя аммиак гипохлоритом натрия в присутствии желатина, получают гидразин:
7) С галогеноалканами аммиак вступает в реакцию нуклеофильного присоединения, образуя замещённый ион аммония (способ получения аминов):
Соли аммиака:
Соли аммония
- твёрдые кристаллические вещества, не имеющие окраски. Почти все они растворяются в воде, и им характерны все те же свойства, которые имеют известные нам соли металлов. Они взаимодействуют со щелочами, при этом выделяется аммиак.
NH 4 Cl + KOH -> KCl + NH 3 + H 2 O
При этом, если дополнительно воспользоваться индикаторной бумагой, то эту реакцию можно использовать - как качественную реакцию на соли аммония
. Соли аммония взаимодействуют с другими солями и кислотами. Например,
(NH 4) 2 SO 4 + BaCl 2 -> BaSO 4 + 2NH 4 Cl
(NH 4) 2 CO 3 + 2HCl 2 -> 2NH 4 Cl + CO 2 + H 2 O
Соли аммония
неустойчивы к нагреванию. Некоторые из них, например хлорид аммония (или нашатырь), - возгоняются (испаряются при нагревании), другие, например нитрит аммония, - разлагаются
NH 4 Cl -> NH 3 + HCl
NH 4 NO 2 -> N 2 + 2H 2 O
Последняя химическая реакция - разложение нитрита аммония - используется в химических лабораториях для получения чистого азота.
Азотоводородная кислота, соли азиды. Азо́тистоводоро́дная кислота́ , азоими́д , HN 3 - кислота, соединение азота с водородом. Бесцветная, летучая, чрезвычайно взрывоопасная (взрывается при нагреве, ударе или трении) жидкость с резким запахом. Очень токсична. Её хорошо растворимые соли тоже очень ядовиты. Механизм токсичности аналогичен цианидам (блокирование цитохромов). Азиды- химические соединения, содержащие одну или несколько групп - N 3 , производные азотистоводородной кислоты (См.Азотистоводородная кислота) HN 3 . К неорганическим А. относятся соли HN 3 [например, А. натрия NaN 3 , А. свинца Pb(N 3) 2 ], галогеназиды (например, хлоразид CIN 3) и др. Большинство неорганических А. взрывается при лёгком ударе или трении даже во влажном состоянии; таков, например, Азид свинца, применяющийся как инициирующее взрывчатое вещество. Исключение составляют NaN 3 и др. соли щелочных и щёлочноземельных металлов. Исходным материалом для получения др. солей HN 3 , а также самой кислоты обычно служит А. натрия, получаемый пропусканием закиси азота через расплавленный амид натрия: NaNH 2 + ON 2 = NaN 3 +H 2 O. Все органические А., алкильные и арильные (общей формулы RN 3) или ацильные ( 2)N 3 .
Амиды, имиды и нитриды металлов.
Амиды металлов MeNH 2 - соединения, содержащие ионы NH 2 − . Амиды являются аналогами гидроксидов, но являются более сильными основаниями. Некоторые амиды растворяются в аммиаке, причем амид растворим в аммиаке так же, как и гидроксид этого металла в воде. Аммиачные растворы амидов проводят электрический ток.В амиде один или два атома водорода могут быть замещены на органические радикалы, как, например, в диизопропиламиде лития LiN(C 3 H 7) 2
ИМИДЫ МЕТАЛЛОВ
-соед. общей ф-лы М2/nNН, где п - степень окисления металла М. Легко гидролизуются водой, образуя гидроксид металла и NH3. При нагр. переходят в нитриды металлов или разлагаются на своб. металл, N2 и Н2. Получают имиды металлов нагреванием амидов металлов в вакууме при 400-600 °С. Известно небольшое число имидов металлов. Наиб. изучен имид лития Li2NH, к-рый существует в двух кристаллич. модификациях; до 83 °С устойчива форма с тетрагон. решеткой (а = 0,987 нм, b = 0,970 нм, с = 0,983 нм, z = 16; плотн. 1,20 г/см3), выше 83°С - с кристаллич. решеткой типа антифлюорита (плотн. 1,48 г/см3). Получено множество орг. производных имидов металлов, в к-рых атом водорода замещен на орг. pадикал. П. И.Чукуров.
Нитриды
- соединения азота с менее электроотрицательными элементами, например, с металлами (AlN;TiN x ;Na 3 N;Ca 3 N 2 ;Zn 3 N 2 ; и т. д.) и с рядом неметаллов (NH 3 , BN, Si 3 N 4).
Соединения азота с металлами чаще всего являются тугоплавкими и устойчивыми при высоких температурах веществами, например, эльбор. Нитридные покрытия придают изделиям твёрдость, коррозионную стойкость; находят применение в энергетике, космической технике.
Биологическая роль азота. Ч истый (элементарный) азот сам по себе не обладает какой-либо биологической ролью. Биологическая роль азота обусловлена его соединениями. Так в составе аминокислот он образует пептиды и белки (наиболее важный компонент всех живых организмов); в составе нуклеотидов образует ДНК и РНК (посредством которых передается вся информация внутри клетки и по наследству); в составе гемоглобина участвует в транспорте кислорода от легких по органам и тканей.
атрия тиосульфат Natrii thiosulfas
Na 2 S 2 0 3 -5H 2 0 M. м. 248,17
Натрия тиосульфат не является природным продуктом, его получают синтетически.
В промышленности натрия тиосульфат получают из отходов газового производства. Этот метод несмотря на многостадий-ность экономически выгоден, так как сырьем являются отходы газового производства и, в частности, светильный газ, образу-ющийся при коксовании угля.
Светильный газ всегда содержит примесь сероводорода, ко-торый улавливается поглотителями, например гидроксидом кальция. При этом получается сульфид кальция.
Но сульфид кальция в процессе получения подвергается гидролизу, поэтому реакция идет несколько иначе -с обра-зованием гидросульфида кальция.
Гидросульфид кальция при окислении кислородом воздуха образует тиосульфат кальция.
При сплавлении полученного тиосульфата кальция с сульфа-том натрия или карбонатом натрия получается тиосульфат нат-рия Na 2 S 2 0 3 .
![]()
После упаривания раствора выкристаллизовывается тио-сульфат натрия, который и является фармакопейным препара-том.
По внешнему виду тиосульфат натрия (II) представляет со-бой бесцветные прозрачные кристаллы солоновато-горького вкуса. Очень легко растворим в воде. При температуре 50 °С плавится в своей кристаллизационной воде. По структуре яв-ляется солью тиосерной кислоты (I).

Как видно из формулы этих соединений, степень окисления атомов серы в их молекулах различна. Один атом серы имеет степень окисления +6, другой -2. Присутствие атомов серы в различных степенях окисления обусловливает их свойства.
Так, имея в молекуле S 2- , натрия тиосульфат проявляет вос-становительную способность.
Как и сама тиосерная кислота, соли ее не являются проч-ными соединениями и легко разлагаются под влиянием кислот и даже таких слабых, как угольная.

Это свойство натрия тиосульфата разлагаться кислотами с выделением серы используется для идентификации препарата. При добавлении к раствору натрия тиосульфата хлороводород-ной кислоты наблюдается помутнение раствора вследствие вы-деления серы.

Весьма характерной для натрия тиосульфата является реак-ция его с раствором нитрата серебра. При этом выделяется осадок белого цвета (тиосульфат серебра), который быстро желтеет. При стоянии под влиянием влаги воздуха осадок чер-неет вследствие выделения сульфида серебра.
Если при действии на натрия тиосульфат нитратом серебра сразу образуется черный осадок, это указывает на загрязнение препарата сульфидами, которые при взаимодействии с нитра-том серебра сразу выделяют осадок сульфида серебра.

Чистый препарат при действии раствора нитрата серебра темнеет не сразу.
В качестве реакции подлинности может быть использована также реакция взаимодействия натрия тиосульфата с раство-ром хлорида железа (III). При этом образуется тиосульфат окисного железа, окрашенный в фиолетовый цвет. Окраска бы-стро исчезает вследствие восстановления этой соли до бесцвет-ных солей закисного железа (FeS 2 0 3 и FeS 4 0 6).
При взаимодействии с йодом натрия тиосульфат действует как восстановитель. Принимая электроны от S 2- , йод восста-навливается до I - , а натрия тиосульфат окисляется йодом до тетратиоиата натрия.

Аналогично восстанавливается хлор в хлороводород.

При избытке хлора выделяющаяся сера окисляется до сер-ной кислоты.
На этой реакции было основано применение натрия тиосуль-фата для поглощения хлора в первых противогазах.
В препарате не допускается наличие примесей мышьяка, се-лена, карбонатов, сульфатов, сульфидов, сульфитов, солей каль-ция.
ГФ X допускает наличие примесей хлоридов, солей тяжелых металлов в пределах эталона.
Количественное определение натрия тиосульфата проводят йодометрическим методом, в основу которого положена реак-ция его взаимодействия с йодом. ГФ требует содержания тио-сульфата натрия в препарате не менее 99% и не более 102% (за счет допустимого предела выветривания препарата).
Применение натрия тиосульфата основано на его свойстве выделять серу. Препарат применяется в качестве противоядия при отравлениях галогенами, цианом и циановодородной кис-лотой.

Образующийся роданид калия гораздо менее ядовит, чем цианид калия. Поэтому при отравлении циановодородной кис-лотой или ее солями в качестве первой помощи следует при-менить натрия тиосульфат. Препарат может применяться также при отравлении соединениями мышьяка, ртути, свинца; при этом образуются неядовитые сульфиды.
Натрия тиосульфат применяется также при аллергических заболеваниях, артритах, невралгии - внутривенно в виде 30% водного раствора. В связи с этим ГФ X приводит 30% раствор натрия тиосульфата для инъекций (Solutio Natrii thiosulfatis 30% pro injectionibus).
Выпускается в порошках и в ампулах по 5, 10, 50 мл 30% раствора.
Натрия тиосульфат содержит кристаллизационную воду, ко-торая легко выветривается, поэтому хранить ее следует в про-хладном месте, в хорошо закупоренных склянках из темного стекла, так как свет способствует его разложению. Растворы при стоянии мутнеют от выделяющейся серы. Этот процесс ускоряется в присутствии диоксида углерода. Поэтому склянки или бутыли с растворами натрия тиосульфата снабжаются хлоркальциевой трубкой, наполненной натронной известью, ко-торая ее поглощает.
Тема: СКОРОСТЬ ХИМИЧЕСКИХ РЕАКЦИЙ И
ХИМИЧЕСКОЕ РАВНОВЕСИЕ
Зависимость скорости реакции от температуры
(проверка правила Вант-Гоффа)
Закономерность изучается на примере взаимодействия тиосульфата натрия с серной кислотой
Реакция протекает в две стадии:
Первая стадия - ионный обмен - происходит мгновенно, так что фактически наблюдение ведётся за скоростью второй мономолекулярной стадии, признаком протекания которой является появления мути как результат образования элементарной серы. Поэтому концентрации серной кислоты фактически не сказывается на скорости реакции, лишь бы она была взята в количестве, достаточном для полного взаимодействия тиосульфата, и во всех опытах одинакова.
Следовательно, уравнение скорости может быть записано так:
Опыт 1 . Приготовить простейший термостат: стакан на 200 мл с крышкой, в которой имеются 3 отверстия. В первое отверстие опустить закрепленный на нитке термометр, во второе - коническую пробирку с -2н раствором Н 2 SO 4 с опущенной в неё пипеткой, в третье - коническую пробирку, в которую чистой пипеткой внести 10 капель 0,1-н раствора тиосульфата натрия. Стакан заполнить выдержанной при комнатной температуре водой настолько, чтобы шарик термометра и раствора были в неё погружены. Ртутный шарик термометра и растворы реагирующих веществ должны находиться на одном уровне в средней части воды, заполняющей стакан - термостат.
Выждав 5 минут – время, необходимое для выравнивания температуры воды в термостате и растворов в пробирках, записать показания термометра. Не вынимая пробирки из термостата, к раствору тиосульфата натрия добавить пипеткой 1 каплю раствора серной кислоты. В этот момент включить секундомер (замерить время по часам с секундной стрелкой), не вынимая пробирку из термостата, наблюдать за ходом опыта до появления в пробирке заметного на глаз помутнения и при обнаружении его выключить секундомер. Записать длительность опыта в секундах.
Опыт 2. Проводится при температуре, повышенной на 10°. Для этого пробирку в термостате, в которой проводился опыт, заменить чистой и вновь внести в неё 10 капель 0,1н раствора тиосульфата натрия. Добавляя в стакан горячую воду, поднять её температуру на 14 - 15° выше температуры первого опыта и по термометру наблюдать её охлаждение. Когда температура будет на 10° выше, провести опыт точно так же, как первый.
Опыт 3. Проведение опыта при температуре, повышенной на 20°. Опыт проводиться так же, как в предыдущем случае, но температура воды в термостате первоначально повышается на 24 - 25°выше комнатной, а добавление серной кислоты к гипосульфиту производится в тот момент, когда она будет выше температуры первого опыта ровно на 20°. Все опытные данные и результаты расчетов записываются в виде таблицы. Вместо индексов указать фактические температуры.
Вычислить:
А) относительную скорость реакции.
Примем скорость реакции при комнатной температуре
в первом опыте. Поскольку скорость и величина, обратная времени,
из этой пропорции находим
Аналогично составляем пропорцию и вычисляем
Б) термический коэффициент скорости по Вант - Гоффу. Его вычисляют по результатам двух опытов, независимо один от другого.
Выполнение работы является удовлетворительным в том случае, если результаты этих двух вычислений расходятся незначительно. Тогда можно взять их средние значения. При резком расхождении работу нужно повторить.
Скорость химических реакций в гомогенных и
ГЕТЕРОГЕННЫХ СИСТЕМАХ
Опыт 1. Влияние величины поверхности раздела реагирующих веществ на скорость реакции в гетерогенной системе
Растворение карбоната кальция в хлороводородной кислоте
Выполнение работы . Взять два небольших, по возможности одинаковых, кусочка мела. Один из них положить на кусочек фильтровальной бумаги и стеклянной палочкой измельчить его в порошок. Полученный порошок поместить в коническую пробирку. Второй кусочек мела целиком опустить в другую коническую пробирку. В обе пробирки одновременно добавить одинаковое количество (10-20 капель) хлороводородной кислоты плотностью - 1,19 г/см 3 . (Для соблюдения одновременности добавления кислоты опыт могут проводить два студента совместно). Отметить время полного растворения мела в каждом случае.
Запись данных опыта.
Написать уравнение соответствующей
реакции. Почему скорость растворения мела в этих двух случаях
различна?
Опыт 2. Влияние катализатора на скорость реакции
Каталитическое восстановление железа (III) Выполнение работы. В две пробирки внести по 10 капель 0,5 н. раствора роданида калия и по 1 капле 0,5 н. раствора…Опыт 3. Смещение химического равновесия обратимых реакций
Влияние концентрации реагирующих веществ на смещение равновесия Выполнение работы. В четыре конические пробирки внести по 5-7 капель 0,0025 н. растворов хлорида железа (III) и…ТЕМА: РАСТВОРЫ
Опыт 1 Определение плотности раствора ареометром.
Рисунок 1- Ареометр для определения плотности раствораОпыт 2 Приготовление растворов различной концентрации
А) Приготовление 0,1н раствора серной кислоты.
2. Сколько мл 10% раствора серной кислоты (ρ, см. опыт №1) необходимо взять для приготовления 250мл 0,1н раствора серной кислоты. 3. Сколько мл 15% раствора серной кислоты (ρ, см. опыт №1) необходимо… 4. Сколько мл 15% раствора серной кислоты (ρ, см. опыт №1) необходимо взять для приготовления 250мл 0,1н раствора…Б) Приготовление раствора заданной концентрации смешением растворов более высокой и более низкой концентрации
2. Приготовить 150 мл 12%-ного раствора гидроксида натрия, имея в своем, распоряжении 5%-ный и 25%-ный растворы NaOH. 3. Приготовить 500 мл 20%-ного раствора гидроксида натрия, имея в своем,… 4. Приготовить 250 мл 15%-ного раствора гидроксида натрия, имея в своем, распоряжении 8%-ный и 25%-ный растворы…Опыт 3 Определение концентрации растворов
Бюретку вместимостью 10 мл (рисунок 2в) промыть небольшим объемом 0,1н раствора NaOH, после чего вылить ее через нижний конец бюретки, снабженный… В коническую колбочку вместимостью 30-50 мл сухой пипеткой (рисунок 2б) внести… Повторить титрование еще три раза. Резкое изменение окраски фенолфталеина от одной капли щелочи является показателем…ТЕМА: ТЕОРИЯ ЭЛЕКТРОЛИТИЧЕСКОЙ ДИССОЦИАЦИИ
Опыт 1. Сравнение электропроводности растворов некоторых электролитов.
В стакан с электродами налить 20-30 мл дистиллированной воды. Загорается ли лампочка? Проводит ли вода электрически ток? Внести в стакан с водой 4-5… Объяснить, почему раствор соли является проводником тока, хотя чистая вода и… В четыре стакана вместимостью 50 мл каждый налить по 20-30 мл 0,1 н. растворов: в первый – хлороводородной кислоты, во…Опыт 2. Характер диссоциации гидроксидов
Выполнение работы. Пронумеровать 5 пробирок и внести по 4-5 капель 0,5 н. растворов: в первую пробирку MgCl2 , во вторую- AlCl3 , в третью… Аналогичным образом исследовать свойства гидроксидов алюминия, кремния, никеля(II) и цинка. В чем они растворяются?…Опыт 3. Сравнение химической активности кислот
а) Взаимодействие хлороводородной и уксусной кислот с мрамором. Выполнение работы.В одну пробирку внести 3-4 капли 2н. раствора уксусной кислоты, в другую – столько же 2 н. раствора…Опыт 4. Смещение равновесия диссоциации слабых электролитов
а) Влияние соли слабых кислот на диссоциацию этой кислоты Выполнение работы. В две пробирки по 5-7 капель 0,1 н. раствора уксусной кислоты. В каждую пробирку прибавить одну…Опыт 1. Реакция среды в растворах различных солей
Растворы размешать (стеклянные палочки не переносить из одного раствора в другой). По изменению окраски лакмуса сделать вывод о реакции среды в растворе каждой… Какие из исследованных солей подвергаются гидролизу? Написать ионные и молекулярные уравнения реакций их гидролиза и…Опыт 2. Образование основных и кислых солей при гидролизе
А) Гидролиз сульфита натрия
На присутствие каких ионов в растворе указывает найденное значение pH? В результате какого процесса эти ионы появились? По отсутствию запаха сернистого газа убедиться в том, что сульфит натрия… Написать молекулярное и ионное уравнения реакции гидролиза сульфита натрия. При гидролизе каких солей получаются…Опыт 3. Факторы, влияющие на степень гидролиза солей
A) Влияние силы кислоты и основания, образующих соль, на степень её гидролиза
Написать ионные уравнения гидролиза сульфита натрия и карбоната натрия (по первой ступени). В растворе какой соли окраска фенолфталеина более… Степень гидролиза какой соли при одинаковых концентрациях и температуре должна… Сделать общий вывод о влиянии силы кислоты и основания, образующих соль, на степень её гидролиза.ТЕМА: ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ
ПРОЦЕССЫ
ВОДОРОД
Опыт 1 Получение водорода
Открыть кран газоотводной трубки. Наблюдать, как кислота вливается в аппарат, заполняет нижнюю часть его и поднимается в среднюю, где находится… Ознакомиться с автоматичностью действия аппарата Киппа. Для этого закрыть кран… НИКОГДАне зажигать водород на конце газоотводной трубки аппарата Киппа, не проверив его на чистоту и не будучи…ПРОВЕРКА ЧИСТОТЫ ВОДОРОДА
Опыт 2 Переливание водорода.
Проверить чистоту водорода и наполнить им большую пробирку, держа её вверх дном, поместить с ней рядом, тоже вверх дном, другую пробирку так, чтобы их отверстия были рядом. Не отодвигая пробирки с водородом, повёртывать её вниз дном так, чтобы пустая пробирка накрыла бы пробирку с водородом. Разъединив пробирки, поднести каждую из них к пламени спиртовки. В какой пробирке наблюдается вспышка?
Опыт 3 Образование воды при горении.
ПРОВЕРИТЬ ВОДОРОД на чистоту. Если он чист, зажгите его на конце газоотводной трубки и, держа трубку вверх, накройте пламя стеклянной банкой, прекратив процесс выделения водорода. Что для этого надо сделать? Что наблюдается на стенках банки? Записать уравнение реакции.
КИСЛОРОД
ПОЛУЧЕНИЕ КИСЛОРОДА И СЖИГАНИЕ В НЁМ ВЕЩЕСТВ
1. Ознакомиться с устройством газометра. 2. В пробирку поместить перманганат калия, закрыть пробкой с газоотводной…Опыт 2. Сжигание серы в кислороде.
Опыт 3. Сжигание магния в кислороде.
Наполнить банку кислородом, как в предыдущем опыте. Взять тигельными щипцами стружку или ленту магния, нагревать в пламени спиртовки, пока она не загорится и быстро внести в банку с кислородом. Что собой представляет оксид магния? Испытать характер оксида магния. Для этого, как в предыдущем опыте, влить в банку немного раствора фиолетового лакмуса и взболтать. Как изменился цвет лакмуса? Сделать вывод о характере образующегося гидроксида.
Опыт 4. Сжигание железа в кислороде.
Влияние среды на протекание окислительно - восстановительных процессов Влияние рН среды на характер восстановления перманганата калияH2O2 + 2H+ + 2e- = 2H2O
для реакции окисления пероксида водорода (H 2 O 2 – восстановитель):
H 2 O 2 – 2e - = O 2 + 2H +
б)Взаимодействие пероксида водорода с иодидом калия
Выполнение работы. К раствору иодида калия, подкисленному серной кислотой, прибавить 1 – 2 капли раствора пероксида водорода. Для какого вещества характера появившаяся окраска раствора?
Написать уравнение реакции. Окислителем или восстановителем является в ней пероксид водорода?
в) Взаимодействие пероксида водорода с оксидом ртути (II)
Выполнение работы. Поместить в пробирку 3 – 4 капели раствора нитрата ртути Hg(NO 3) 2 и добавить столько же 2 н. раствора щелочи до выпадения осадка оксида ртути (II). Отметить цвет осадка. Добавить 4 – 5 капель раствора пероксида водорода и наблюдать изменение цвета осадка вследствие образования взвешенных частиц металлической ртути. Какой газ выделяется?
Написать уравнение реакции. Окислитлем и восстановителем является пероксид водорода в данной реакции? Сделать соотвествующие выводы.
ОПРЕДЕЛЕНИЕ ЭЛЕКТРОДНЫХ ПОТЕНЦИАЛОВ. НАПРАВЛЕНИЕ
ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ
ПРОЦЕССОВ
Выполнение работы.Один из микростаканчиков 1 (рисунок) заполнить доверху 1М раствором сульфата цинка (точнее раствором, в котором активность ионов… Запись данных опыта.Изобразить двойной электрический слой на границе раздела металл - раствор его соли на цинковом и…ЭЛЕКТРОЛИЗ ВОДНЫХ РАСТВОРОВ
Описанные ниже опыты проводят в приборе, представленным на рисунке.Б) Электролиз раствора иодида калия
Отметить изменение цвета раствора около катода и анода. Написать уравнение катодного и анодного процессов. Почему окрасились растворы в катодном и…В) Электролиз раствора сульфата натрия
Выполнение работы. В стакане, объемом 100 мл смешать раствор сульфата натрия с нейтральным раствором лакмуса и вылить полученный раствор в…Г) Электролиз водных растворов солей с растворимыми анодами
Выполнение работы . Налить в электролизер 0,5 н. раствор сульфата меди, опустить в него графитовые электроды и пропустить через раствор электрический ток. Через несколько минут прекратить электролиз и отметить на катоде красный налет меди. Написать уравнения катодного и анодного процессов. Какой газ в небольших количествах выделяется на аноде?
Не отключая электролизер от батарейки, поменять местами электроды в коленах электролизера, вследствие чего электрод, покрывшийся вначале медью, окажется анодом. Снова пропустить электрический ток. Что происходит с медью на аноде? Какое вещество выделяется на катоде? Написать уравнения катодного и анодного процессов, протекающих при электролизе сульфата меди с медным анодом.
Провести аналогичный опыт с 0,5 н. раствором сульфата никеля (II). Что выделяется на катоде? Написать уравнение катодного восстановления никеля. Какое вещество окисляется на аноде при электролизе сульфата никеля с угольным анодом? С никелевым анодом? Написать уравнения соответствующих анодных процессов.
ТЕМА: КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ
Опыт 1. Получение и свойства некоторых аммиакатов
Разбавить раствор приблизительно равным объёмом спирта и отцентрифуговать образовавшиеся при этом кристаллы [Сu(NH3)4]SO4 ·H2O – комплексного… Написать уравнения всех реакций, проведённых в этом опыте.Опыт 2. Исследование тетрааминкупро(׀׀) сульфата
В четыре пронумерованные пробирки внести пипеткой по 10 капель исследуемого раствора комплексной соли. а) Проба на ион Cu2+ действием щёлочи. В пробирку №1 добавить несколько капель… б) Проба на ион Cu2+ действием сульфида натрия. В пробирку №2 добавить несколько капель раствора Na2S. Наблюдается ли…ТЕМА: ХИМИЯ ЭЛЕМЕНТОВ
ГАЛОГЕНЫ
Опыт 1. Получение хлора
Выполнение работы. В три пробирки положить по 3-4 кристаллика различных окислителей: в первую диоксида марганца MnO2 или диоксида свинца PbO2, во… а) получение хлора, учитывая, что окислительные числа марганца меняются с +4 в… б) взаимодействия хлора с тиосульфатом натрия с участием воды; реакция протекает с образованием свободной серы,…Опыт 2. Получение хлорной воды и исследование её свойств
А) Получение хлорной воды
Написать уравнение реакции получения хлора окислением соляной кислоты перманганатом калия, учитывая, что окислительное число марганца изменяется от…Б) Исследование состава и свойств хлорной воды
Cl2 + H2O ↔HClO + HCl. (1) При этом равновесие сильно смещено влево. Поэтому хлорной водой можно… HClO = HCl + O (2)Опыт 3. Получение брома
Выполнение работы. В сухую цилиндрическую пробирку поместить 2-3 кристаллика бромида калия или натрия и столько же диоксида марганца. Осторожно встряхнуть пробирку и прибавить к смеси 2-3 капли концентрированной серной кислоты (пл. 1,84 г/см 3). Что представляют собой выделяющиеся бурые пары? Написать уравнение реакции получения брома.
Опыт 4. Получение иода
Опыт 5. Окислительные свойства свободных галогенов (окислительное число равно…А) Сравнение окислительной активности свободных галогенов.
По окраске бензольного кольца определить, какой галоген выделяется в свободном состоянии в каждом случае. Написать уравнения реакций взаимного…Б) Окисление бромом магния или цинка.
Внести впробирку 3 – 5 капель бромной воды и немного порошка магния или цинка. Перемешать стеклянной палочкой. Отметить обесцвечивание растворов бромной водой и указать причину этого явления. Написать соответствующее уравнение реакции.
Опыт 6. Получение водородных соединений галогенов (галогеноводородов).
Галогеноводороды могут быть получены действием нелетучих и не являющихся окислителями кислот на галиды металлов.
Б) Действие плавиковой кислоты на стекло.
В) Получение хлороводорода и его растворение в воде.
Наполнив пробирку сероводородом, плотно закрыть ее пробкой. Отсоединить капилляр от трубки, быстро закрыть его указательным пальцем и, перевернув…Г) Получение бромоводорода и иодоводорода.
Положить в одну пробирку 2-3 микрошпателя бромида кадия или натрия, в другую – столько же какого-либо иодида. В обе пробирки добавить по 5-10 капель концентрированного раствора фосфорной ортокислоты. Подогреть растворы на маленьком пламени горелки. Наблюдать выделение бромоводорода и иодоводорода в виде белого дыма. Выделяется ли при этом свободный бром и иод? Сделать вывод, окисляет ли фосфорная кислота бромоводород и иодоводород? Написать уравнения реакций.
Опыт 7. Восстановительные свойства галогеноводородов и галид- ионов.
А) Восстановление серной кислоты.
Отметить во второй пробирке выделение бурых паров брома и диоксида серы SO2, в третьей – фиолетовых паров иода, серы и сероводорода, образующихся… Написать уравнение реакции взаимодействия хлорида, бромида и иодида калия или…Б) Восстановление трихлорида железа.
Могут ли отрицательные ионы галогенов являться окислителями? Ответ обосновать. Опыт 8. Взаимодействие брома с алюминием. В демонстрационную пробирку, закрепленную в штативе над поддоном с песком, налить бром. Опустить в него алюминиевый…Опыт 1. Получение аммиака и исследование его свойств
Опыт 2. Получение оксидов азота и азотной кислоты
а) получения оксида азота (II) взаимодействием разбавленной азотной кислоты с медью; б) окисления оксида азота (II) до оксида азота (IV) и полимеризации оксида… в) взаимодействия диоксида азота с водой, протекающего с образованием азотной и азотистой кислот;Опыт 3. Получение азотистой кислоты и ее распад
а) взаимодействие нитрита калия с серной кислотой; б) разложения азотистой кислоты; в) распад азотистого ангидрида.Опыт 4. Окислительно-восстановительные свойства нитритов
1.Внести в пробирку 2-4 капли раствора иодида калия и столько же 2н серной кислоты. Добавить 2-4 капли раствора нитрита калия или натрия. Чем… 2. Взаимодействие нитрита калия с перманганатом. В пробирку внести 2-3 капли…Опыт 5. Окислительные свойства азотной кислоты
Взаимодействие разбавленной азотной кислоты с медью и оловом
2. Взаимодействие концентрированной азотной кислотой с медью и оловом. В 2 пробирки поместить по маленькому кусочку меди и олова. Прибавить к ним по…Опыт 6 . Соли азотной кислоты
2-3 микрошпателя сухого нитрата калия поместить в цилиндрическую пробирку. Укрепив её наклонно в штативе, нагреть до расплавления соли. Внести…Опыт 1. Аллотропия фосфора
P+CuSO4+H2O H3PO4+H2SO4+CuОпыт 2. Соли фосфорной ортокислоты
Найти константы диссоциации фосфорной ортокислоты и определить, подвергаются ли гидролизу ортофосфаты щелочных металлов. Проверить свои…СЕРА И ЕЕ СВОЙСТВА
Опыт1. Аллотропия серы
1. Получение пластической серы. В пробирку на 10 мл. насыпать на ¼ объема мелких кусочков черенковой серы. Укрепить пробирку в держателе и…Опыт 2. Получение диоксида серы и сернистой кислоты
Микро колбу наполнить на 1/3 ее объема кристаллами сульфата натрия, добавить 6-8 капель 4 и раствора серной кислоты и быстро закрыть пробкой о… Опыт 3. Окислительные и восстановительные свойства серы(IV)Опыт 5. Дегидратирующие свойства серной кислоты
Опыт 6 Теосерная кислота и теосульфаты
1. Исследование тиосерной кислоты. Внести в пробирку 5-6 капель раствора тиосульфата натрия Na2S2O3 и 3-4 капли раствора серной кислоты. Отметить… 2. Взаимодействие тиосульфата натрия с хлором и бромом. В две пробирки с… 3. Взаимодействие тиосульфата натрия с йодом. В пробирку с йодной водой (5-6 капель) прибавить по каплям раствор…ПРИЛОЖЕНИЕ
Таблица 1 - Константы нестойкости некоторых комплексных ионов
| Комплексный ион | К нест |
| - | 1 ∙ 10 -21 |
| + | 7 ∙ 10 -8 |
| 3- | 1 ∙ 10 -13 |
| 2- | 9 ∙ 10 -3 |
| 2- | 8 ∙ 10 -7 |
| 2- | 1 ∙ 10 -17 |
| 2+ | 8 ∙ 10 -8 |
| 2+ | 8 ∙ 10 -6 |
| 3+ | 6 ∙ 10 -36 |
| 2+ | 2 ∙ 10 -13 |
| 3- | 5 ∙ 10 -28 |
| 4- | 1 ∙ 10 -37 |
| 3- | 1 ∙ 10 -44 |
| 2+ | 1 ∙ 10 -3 |
| 2- | 1 ∙ 10 -21 |
| 2- | 8 ∙ 10 -16 |
| 2- | 1 ∙ 10 -30 |
| 2- | 1 ∙ 10 -22 |
| 2- | 3 ∙ 10 -16 |
| 2+ | 2 ∙ 10 -9 |
| 2- | 2 ∙ 10 -17 |
| ] 2+ | 4 ∙ 10 -10 |
Таблица 2 - Плотность растворов некоторых кислот, щелочей и аммиака при 20 0 С (в г/см 3 , г/мл).
Преподаватель: Кораблёва А.А.
ОТЧЕТ
О ЛАБОРАТОРНОЙ РАБОТЕ
ПО КУРСУ: ОБЩАЯ ХИМИЯ
" СКОРОСТЬ РЕАКЦИИ В РАСТВОРАХ "
ОФ 62 5528 1.04 ЛР
Работу выполнил
студент группы
Санкт – Петербург
Цель работы:
Определить константу скорости, температурный коэффициент, энергию активации реакции взаимодействия тиосульфата натрия с серной кислотой.
В данной лабораторной работе изучается реакция между тиосульфатом натрия (гипосульфитом) Na2S2O3 и серной кислотой H2SO4.
Эта реакция протекает в две стадии:
1) (быстро)
Первая стадия ионного обмена протекает практически мгновенно. Тиосерная кислота неустойчивое соединение, распадающееся с выделением белого осадка серы.
2) (медленно)
О скорости реакции можно судить по появлению опалесценции и дальнейшему помутнению раствора от выпавшей серы.
Суммарная реакция определяется второй стадией процесса и зависит от концентрации H2SO4 , а значит и Na2S2O3 (реакция псевдомолекулярна).
 Кинетическое
уравнение имеет вид:
Кинетическое
уравнение имеет вид:
Приборы и реактивы:
Термостаты, термометры, мерные цилиндры, пробирки, пробиркодержатели, секундомер, растворы Na2S2O3 и H2SO4 .
Опыт №1:
Влияние тиосульфата на скорость химической реакции.
Зависимость скорости реакции от концентрации тиосульфата натрия.
Обработка результатов опыта:
Рассчитываем относительную скорость реакции по формуле:
2. Исходя из кинетического уравнения, определяем значение константы скорости реакции:
Р
3. Определяем среднее значение константы для данной комнатной температуры, в данном случае Т = 14 град цельс.
4 .
Выразить зависимость скорости реакции
от концентрации тиосульфата – графически.
(см. рис.№1).
.
Выразить зависимость скорости реакции
от концентрации тиосульфата – графически.
(см. рис.№1).
5. Графически определяем константу скорости реакции как тангенс угла наклона прямой ОА к оси абсцисс. Сравниваем графически определенную константу с ее аналитическим значением.
КГР = tg = 0.162 КСР = 0.17 КГР КСР
Опыт №2:
Влияние температуры на скорость химической реакции.
|
Температура опыта, Т, град цельс. |
реакции t, с |
Относит. скорость реак. V, 1/с |
Конст. скор. реак. К, л/моль*с |
|
Обработка результатов опыта:
1.Рассчитываем относительную скорость реакции при каждой температуре:
Результаты смотреть в вышеприведенной таблице.
2.Исходя из кинетического уравнения определяем значение константы для каждой температуры:
Р езультаты
смотреть в вышеприведенной таблице.
езультаты
смотреть в вышеприведенной таблице.
3.Выражаем графически влияние температуры на скорость химической реакции. (см. рис.№2).
4.Исходя из уравнения Ван-Гоффа определяем для каждого температурного интервала значение температурного коэффициента и вычисляем его среднее значение:
К2/К1 = 1 = 2.42
К3/К2 = 2 = 1.97 сред = 2.3
К4/К3 = 3 = 2.49
5 .
Исходя из уравнения Аррениуса вычисляем
аналитическое значение энергии активации
для каждого температурного интервала:
.
Исходя из уравнения Аррениуса вычисляем
аналитическое значение энергии активации
для каждого температурного интервала:
Е а1
= 61785 Дж/моль Еа2
= 50729 Дж/моль Еа3
=72882 Дж/моль
а1
= 61785 Дж/моль Еа2
= 50729 Дж/моль Еа3
=72882 Дж/моль
И вычисляем его среднее значение:
ЕаСРЕД = 61798 Дж/моль
6. Выстраиваем графическую зависимость lgK от 1/Т по вычисленным константам скоростей при разных температурах и определяем энергию активации графическим способом (см. рис. №3).
tg = - Еа / 2.3 R , следовательно
ЕаГР = -2.3 R tg = -2.3 * 8.3 * tg = 19.09* 3230 = 61660 Дж/моль
7. Сравниваем значения энергии активации полученные графическим и аналитическим путем:
ЕаГР = 61660 Дж/моль ЕаСРЕД = 61798 Дж/моль ЕаГР ЕаГР
Вывод:
При температуре равной const, скорость химической реакции пропорциональна концентрации веществ, участвующих в этой реакции. (см. рис.№1)
С увеличением температуры скорость химической реакции увеличивается
При условии, что концентрация остается неизменной. Это можно объяснить тем, что с ростом температуры атомы веществ переходят в более возбужденное состояние, т. е. они получают дополнительную энергию – энергию активации, необходимую для разрыва химической связи и образования нового вещества.